Cách tính rò rỉ thiết bị
Trong sản xuất, các kỹ sư thường cần sử dụng phương trình trạng thái khí để tính toán hiệu suất của bình áp lực và hệ thống đường ống ở các điều kiện nhiệt độ và áp lực khác nhau, để đảm bảo tính an toàn và hiệu quả của chúng. Thông qua phương trình trạng thái khí, chúng ta có thể hiểu về tốc độ khuếch tán và quy luật phân bố của khí ở các điều kiện khác nhau.
Tương đương khối lượng
Chênh áp do rò rỉ tạo ra phụ thuộc vào khối lượng bên trong của hệ thống đo lường toàn bộ (bao gồm cả vật thể được đo WORK và thiết bị đo). Nó cũng có liên quan mật thiết với thời gian đo lường.
Khi sử dụng máy đo rò rỉ không khí, chúng ta sử dụng một hệ số gọi là tương đương khối lượng (Ve) để biểu thị nguyên nhân của thay đổi áp lực trong hệ thống đo lường toàn bộ (do thay đổi khối lượng bên trong của WORK hoặc cảm biến chênh áp gây ra).
Tương đương khối lượng có thể được tính toán thông qua phương trình sau:
Tùy thuộc vào loại máy đo rò rỉ không khí, có thể sử dụng bộ hiệu chuẩn tự động rò rỉ (ALC) hoặc MASTER rò rỉ để đo trực tiếp giá trị Ve.
Ve = Vw + Vt + {Ks(1 + Vw/Vm) + Kw}(101.3 + P)
Vw = Vm (khối lượng của WORK và MASTER là giống nhau)
Ks = 0.01mL/kPa hoặc 0.005mL/kPa (tùy thuộc vào loại máy)
Kw = 0mL/kPa (khối lượng của WORK không thay đổi)
Trong các điều kiện trên:
Ks(1 + Vw/Vm) + Kw = 2Ks
| Khi Ks = 0.01mL/kPa
Ve = Vw + Vt + 0.02(101.3 + P)
| Khi Ks = 0.005mL/kPa
Ve = Vw + Vt + 0.01(101.3 + P)
Ve: Tương đương khối lượng (mL)
Vw: Khối lượng bên trong của WORK và đường ống (mL)
Vt: Khối lượng bên trong của thiết bị đo (mL), Vt = 9mL
Ks: Tỷ lệ thay đổi khối lượng mỗi đơn vị áp lực của cảm biến (mL/kPa)
Kw: Tỷ lệ thay đổi khối lượng mỗi đơn vị áp lực của WORK
P: Áp lực thử nghiệm (kPa)
Tỷ lệ rò rỉ
Biểu thức mối quan hệ giữa tương đương khối lượng và tỷ lệ rò rỉ Q
pic_setting01
Q: Tỷ lệ rò rỉ (mL/phút) ΔP: Chênh áp (Pa)
Ve: Tương đương khối lượng (mL) T: Thời gian phát hiện (giây)
Ví dụ: Khi tương đương khối lượng là 800mL, thời gian phát hiện là 3 giây, chênh áp đo được là 15Pa. Trong các điều kiện này, tỷ lệ rò rỉ là bao nhiêu?
Chênh áp do rò rỉ có tỷ lệ ngược với tương đương khối lượng.
[Ví dụ]
Khi tỷ lệ tương đương khối lượng là 1 đến 5, chênh áp ở cùng tỷ lệ rò rỉ sẽ là 5 đến 1.
Q: 5mL/phút
T: 2 giây
ΔP1 = 85Pa khi Ve = 200mL
ΔP2 = 17Pa khi Ve = 1000mL pic_setting03
Đặc tính áp lực và khí
a. Áp lực tuyệt đối: Áp lực dựa trên chân không tuyệt đối là điểm tham chiếu
Ví dụ: PaA, kg/cm²A (hoặc kg/cm²abs), Torr (áp lực tuyệt đối = áp lực khí quyển + áp lực biểu)
b. Áp lực biểu: Áp lực dựa trên áp lực khí quyển là điểm tham chiếu
(Áp lực dương/áp lực âm) Ví dụ: PaG, kg/cm²G
c. Chênh áp: Sự khác biệt giữa hai áp lực Ví dụ: PaD, kg/cm²D
Đơn vị áp lực
1bar = 0.1MPa = 1.01972kg/cm², 1Pa = 1N/m², 1Torr = 1mmHg
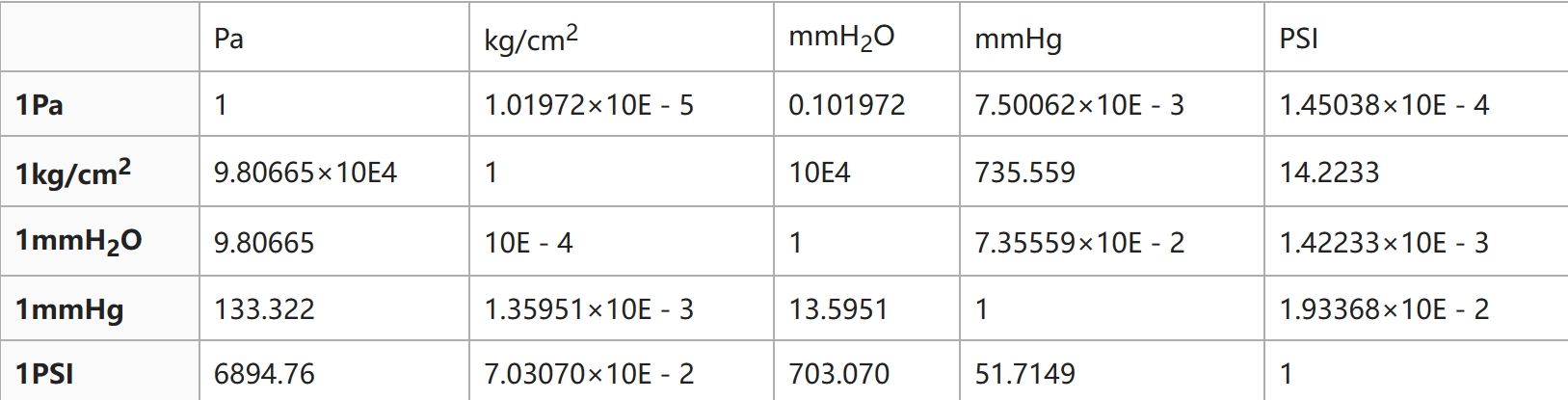
Bảng chuyển đổi đơn vị:
Pa kg/cm² mmH₂O mmHg PSI
1Pa 1 1.01972×10^-5 0.101972 7.50062×10^-3 1.45038×10^-4
1kg/cm² 9.80665×10^4 1 10^4 735.559 14.2233
1mmH₂O 9.80665 10^-4 1 17.35559×10^-2 1.42233×10^-3
1mmHg 133.322 1.35951×10^-3 13.5951 1 11.93368×10^-2
1PSI 6894.76 7.03070×10^-2 703.070 51.71491 1
Chú ý: "10E-3" biểu thị 10 mũ âm ba.
Phương trình trạng thái khí
Giữa áp lực, khối lượng và nhiệt độ của khí có một mối quan hệ bất biến. Một khi hai giá trị trong số đó được xác định, thì giá trị còn lại cũng được xác định theo đó.
Phương trình mô tả mối quan hệ giữa ba giá trị này được gọi là phương trình trạng thái, dựa trên "tổ hợp định luật khí".

PV = GRT …………(1)
Trong phương trình này:
P: Áp lực tuyệt đối
V: Khối lượng
G: Khối lượng khí (hoặc số mol)
T: Nhiệt độ tuyệt đối
R: Hằng số khí
Đối với trạng thái ban đầu (V1, P1, T1) và trạng thái cuối cùng (V2, P2, T2), có các trường hợp đặc biệt sau:
Nếu nhiệt độ giữ nguyên (T1 = T2), thì:
P1 ⋅ V1 = P2 ⋅ V2 ………(2)
Điều này được gọi là Định luật Boyle (Boyle's Law).
Nếu khối lượng giữ nguyên (V1 = V2), thì:
P1 / T1 = P2 / T2 ………(3)
Điều này được gọi là Định luật Charles (Charles' Law).
Chú ý: Trong thực tế, chúng ta thường sử dụng phương trình trạng thái khí lý tưởng PV = nRT, trong đó n là số mol khí, R là hằng số khí chung (giống nhau đối với tất cả các loại khí). Nhưng trong phương trình trên, G được sử dụng để biểu thị khối lượng hoặc số mol khí, và trong hầu hết các ứng dụng kỹ thuật và khoa học, sử dụng số mol và hằng số khí chung là phương pháp phổ biến hơn.
 Cách tính rò rỉ thiết bị
Cách tính rò rỉ thiết bị
 Ưu điểm của máy đo độ kín khí
Ưu điểm của máy đo độ kín khí
 Ống giảm thanh xe bị rò rỉ nướ
Ống giảm thanh xe bị rò rỉ nướ
 Phương pháp kiểm tra độ kín kh
Phương pháp kiểm tra độ kín kh



